Способы получения одноосновных карбоновых кислот ароматического ряда
Рефераты по химии / Синтез нитробензойной кислоты / Способы получения одноосновных карбоновых кислот ароматического рядаСтраница 1
Одноосновные карбоновые кислоты ароматического ряда могут быть получены всеми общими способами, известными для кислот жирного ряда.
Окисление алкильных групп гомологов бензола.
Это один из наиболее часто применяемых способов получения ароматических кислот:
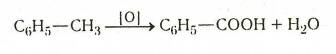
Окисление проводят либо при кипячении углеводорода с щелочным раствором перманганата калия, либо при нагревании в запаянных трубках с разбавленной азотной кислотой. Как правило, этот метод дает хорошие результаты. Осложнения бывают только в тех случаях, когда при действии окислителей разрушается бензольное кольцо.
Окисление ароматических кетонов
. Ароматические кетоны легко получаются реакцией Фриделя — Крафтса. Окисление обычно ведут с помощью гипохлоритов по схеме:
![]()
Однако могут быть использованы и другие окислители. Ацетопроизводные окисляются легче, чем углеводороды.
Гидролиз тригалогенопроизводных с галогенами у одного углеродного атома. При хлорировании толуола образуется три вида хлоропроизводных: хлористый бензил (идет для получения бензилового спирта), хлористый бензилиден (для получения бензойного альдегида), бензотрихлорид (перерабатывается в бензойную кислоту и в хлористый бензоил). Непосредственный гидролиз бензотрихлорида идет плохо. Поэтому бензотрихлорид нагреванием с бензойной кислотой превращают в хлористый бензоил, который далее при гидролизе легко дает бензойную кислоту:
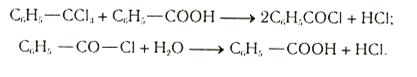
Гидролиз нитрилов:

Этот способ широко применяется в жирном ряду. В ароматическом ряду исходные нитрилы получают из диазосоединений, из галогенопроизводных обменом с цианидом меди в пиридине или сплавлением сульфонатов с цианидом калия. Нитрилы кислот с нитрильной группой в боковой цепи получают обменной реакцией из галогенопроизводных.
Реакция ароматических углеводородов с галогенопроизводными угольной кислоты.
Карбоксильную группу можно ввести в ядро посредством реакции, аналогичной синтезу кетонов по Фриделю — Крафтсу. Катализатором служит хлорид алюминия:
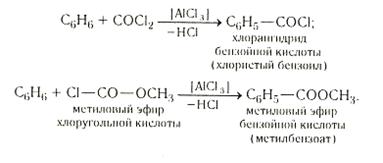
Реакции металлорганических соединений с СО2:
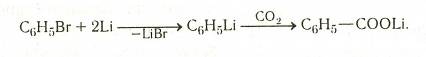 Обычно исползуются литий- или магнийорганические соединения.
Обычно исползуются литий- или магнийорганические соединения.
Химические свойства
Ароматические кислоты вступают во все те реакции, которые свойственны и кислотам жирного ряда. Реакциями с участием карбоксильной группы получают различные производные кислот. Соли получают действием кислот на карбонаты или щелочи.Эфиры — нагреванием смеси кислоты и спирта в присутствии минеральной (обычно серной) кислоты:

Если заместителей в орто-положении нет, то этерификация карбоксильной группы происходит так же легко, как в случае алифатических кислот. Если одно из орто-положений замещено, скорость этерификации сильно уменьшается, а если оба орто-положения заняты, этерификация обычно не идет (пространственные затруднения).
Эфиры орто-замещенных бензойных кислот могут быть получены реакцией солей серебра с галогеналкилами (эфиры пространственно затрудненных ароматических кислот легко и количественно омыляются в присутствии краун-эфиров). Вследствие пространственных затруднений они с трудом подвергаются гидролизу. Группы большие, чем водород, в такой степени заполняют пространство вокруг углеродного атома карбоксильной группы, что затрудняют образование и омыление эфира.
Гидролиз эфиров ароматических кислот, так же как и гидролиз эфиров алифатических кислот, идет как в кислой, так и в щелочной среде. При проведении гидролиза в щелочной среде электроноакцепторные заместители увеличивают скорость гидролиза, а электронодонорные замедляют реакцию. В связи с этим константа ρ в уравнении Гаммета для реакционных серий м- и п-замещеных эфиров имеет положительное значение. Зависимость констант скорости гидролиза от величин σ представлена:

Хлорангидриды получают действием на кислоты хлористого тионила или пентахлорида фосфора:
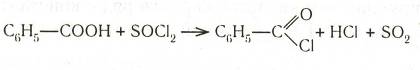
Информация о химии
Коссель (Kossel), Вальтер
Немецкий физик Вальтер Коссель родился в Берлине в известного физиолога, лауреата Нобелевской премии по медицине и физиологии 1910 г. Альбрехта Косселя. Коссель окончил Гейдельбергский университет, где изучал физику у таких выдающ ...
Онзагер (Onsager), Ларс
Норвежско-американский химик Ларс Онзагер родился в Осло, в семье Эрлинга Онзагера, адвоката Верховного суда Норвегии, и Ингрид (Киркеби) Онзагер. Посещая школу в Осло, он изучал литературу, норвежские саги, философию и искусство. ...
Kr — Криптон
КРИПТОН (лат. Krypton), Kr, химический элемент VIII группы периодической системы, атомный номер 36, атомная масса 83,80, относится к инертным, или благородным, газам. Свойства: плотность 3,745 г/л, tкип 153,35 °С. Название: ...


