Получение коллоидных растворов
Рефераты по химии / Получение коллоидных растворовСтраница 1
ЛАБОРАТОРНАЯ РАБОТА № 1
Опыт № 1. Получение коллоидных растворов
Оборудование и реактивы: Химический стакан, пипетка, дистиллированная вода, электрическая плитка, раствор хлорида железа (III) массовой долей 5 %.
Ход работы: В химическом стакане на электрической плитке нагревают воду до кипения. Затем в кипящую воду по каплям приливают немного раствора хлорида железа (III). В кипящем разбавленном растворе гидролиз FeCl3 усиливается. Образуется гидроксид железа (III), который не осаждаетсяна дно стакана: Fe3+ + 3 H2O ® Fe (OH)3 + 3H+.
В результате получается прозрачный коллоидный раствор красно-коричневого цвета состава: {[Fe(OH)3]m , n Fe3+, 3(n-x)Cl-} 3xCl-.
Утилизация. К коллоидному раствору добавить несколько капель соляной кислоты массовой долей 5 %. Полученный раствор хлорида железа использовать в качестве реактива.
Опыт № 2. Прохождение луча света через истинные растворы и коллоидные системы
Оборудование и реактивы: Коллоидный раствор гидроксида железа (III), истинный раствор NaCl, фонарик, два химических стакана, ящик с двумя отверстиями.

Рис. 1. Прохождение луча света через истинные и коллоидные растворы.
Ход работы: В деревянный ящик ставят поочередно истинный раствор NaCl и коллоидный раствор Fe(OH)3. В отверстие ящика направляют луч света от фонарика. В другое отверстие сбоку наблюдают прохождение луча света через растворы. Отмечают, что истинный раствор оптически пуст, а через коллоидный раствор луч света проходит, оставляя «светлую дорожку».
Утилизация. См. опыт № 1.
Опыт № 3. Окислительные свойства хлора по отношению к бромид и иодид ионам
Вариант № 1.
Оборудование и реактивы: Пробирка с резиновыми вставками, хлоркальциевая трубка с активированным углем, штатив, спиртовка, хлорная вода, растворы KI и KBr массовой долей 5 %, раствор крахмала.
Ход работы: В пробирку (рис. 2.) наливаем свежеприготовленной хлорной воды (1). Вставляем в пробирку приготовленные резиновые кружочки- держатели (2) с отверстиями. В первый помещаем слой ваты, смоченный раствором KI и крахмала (3), во второй – слой ваты, смоченный раствором KBr (4). Закрываем пробирку хлоркальциевой трубкой, заполненной углем (5). Подогреваем хлорную воду в пробирке. Выделяющийся хлор реагирует с растворами KI и KBr. Наблюдается изменение окраски: слой ваты с бромидом калия приобретает красновато–коричневый цвет, вата с иодидом калия – синеет: 2KBr + Cl2 ® 2KCl + Br2, 2KI + Cl2 ® 2KCl + I2.

Рис. 2. Окисление хлором бромид и иодид ионов.
Техника безопасности: Установку мыть под вытяжкой, залив ее предварительно щелочным раствором гидроксида кальция.
Утилизация. Промывные воды слить в емкость-нейтрализатор.
Вариант № 2.
Оборудование и реактивы: Пробирка Вюрца с пробкой, две U-образные трубки, хлоркальциевая трубка с активированным углем, штатив, спиртовка, спички, соляная кислота (конц.), KMnO4 (кристал.), ложечка для сжигания, растворы KI и KBr массовой долей 5%.
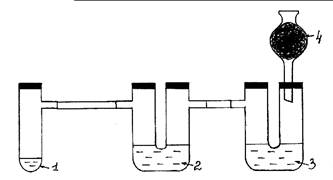
Рис. 3. Окисление хлором бромид и иодид ионов.
Ход работы: Собирают прибор согласно рис. 3. Установка должна быть герметичной. В пробирку Вюрца (1) помещают одну или две ложечки для сжигания кристаллического KMnO4 и соляную кислоту (конц.), немного превышающую уровень соли. Пробирку быстро закрывают пробкой. Выделяющийся хлор проходит сквозь толщу раствора KI в первой U-образной трубке (2). Наблюдают появление коричневой окраски и образование темно- фиолетовых кристаллов. Далее хлор проходит через раствор KBr во второй U–образной трубке (3), окисляя анион брома соли. Раствор приобретает красновато-бурый цвет. Излишки хлора поглощаются активированным углем в хлоркальциевой трубке (4). Закончив опыт, установку переносят в вытяжной шкаф, где проводят утилизацию растворов.
Техника безопасности: Концентрированную соляную кислоту необходимого объема наливают в емкость в вытяжном шкафу, закрывают пробкой и переносят на демонстрационный стол.
Утилизация. В первой по ходу хлора U–образной трубке получают: 2KI + Cl2 ® I2 + 2KCl.
Кристаллы йода оседают через некоторое время на дно трубки, а над осадком получается раствор йода в солевом растворе. Раствор йода слить в склянку и использовать для обнаружения непредельных углеводородов. Кристаллы йода промыть холодной водой, а затем растворить в спирте. Получают спиртовую настойку йода. Если необходим кристаллический йод, то йод высушивают на воздухе, затем переносят в склянку с плотно притертой пробкой. Во второй U–образной трубке получают бром: 2KBr + Cl2 ® Br2 + 2KCl.
Информация о химии
Неорганическая химия
Неоргани́ческая хи́мия — раздел химии, связанный с изучением строения, реакционной способности и свойств всех химических элементов и их неорганических соединений. Это область охватывает все химические соединения, з ...
Штаудингер (Staudinger), Герман
Немецкий химик Герман Штаудингер родился в Вормсе, в семье профессора философии Франца Штаудингера и Августы (Венк) Штаудингер. Штаудингер решил стать ботаником, но отец посоветовал ему прежде изучить химию, считая, что знание это ...
Cr — Хром
ХРОМ (лат. Chromium), Cr, химический элемент VI группы Периодической системы Менделеева, атомный номер 24, атомная масса 51,9961. Свойства: голубовато-серебристый металл; плотность 7,19 г/см3, tпл 1890 °С. На воздухе не окисл ...


