Радикальная сополимеризация акрилат- и метакрилатгуанидинов с виниловыми мономерами
Рефераты по химии / Радикальная сополимеризация акрилат- и метакрилатгуанидинов с виниловыми мономерамиСтраница 3
Детальное исследование кинетических особенностей и закономерностей радикальной полимеризации АК и МАК в водных растворах показало, что зависимость скоростей полимеризации указанных мономеров от рН реакционного раствора имеют вид, указанный на рис. 2.
Так, при полимеризации АК и МАК в водных средах, в интервале рН = = 2,5-7,0 наблюдается значительное падение скорости полимеризации соответствующих мономеров. Значения ММ образующихся полимеров изменяются симбатно. В соответствии со значением констант ионизации для АК рka= 4,2, а для МАК рka = 4,32 (эффективная константа ПАК рka = 6,4, ПМАК рka = 7,0), можно заключить, что в области pH < 6 с увеличением pH реакционного раствора при полимеризации АК и МАК рост цепей происходит на незаряженных макрорадикалах поликислоты. В области рН > 6 зависимость общей скорости полимеризации акрилат- и метакрилатанионов от рН, как было показано на рис. 2, носит экстремальный характер. С ростом рН в области рН = 7-11 и 7-12 соответственно, наблюдается возрастание общей скорости полимеризации и ММ образующихся полимеров. Важно, что скорость инициирования в интервале рН = 8-10 как в присутствии, так и в отсутствие низкомолекулярных неполимеризующихся солей, практически неизменна [15, 16].
Таким образом, наблюдаемое увеличение общей скорости полимеризации акрилат- и метакрилатанионов при возрастании рН в щелочной области или при увеличении ионной силы при фиксированном рН, как выяснилось, действительно вызвано возрастанием отношения констант скоростей элементарных реакций роста и обрыва цепей, т.е. величины kр/kо1/2.
На основании рассмотрения литературных и экспериментальных данных В.А.Кабанов и Д.А.Топчиев [14, 19-20], выдвинули гипотезу о кинетической роли ионных пар при радикальной полимеризации ионизирующихся мономеров. Для случаев полимеризации акрилат- и метакрилатанионов в водных растворах эта гипотеза была сформулирована и обоснована следующим образом. В водных растворах при рН > 7 АК и МАК полностью
 Рис. 1. Зависимость V/Vмин от рН при полимеризации АК в водных растворах.
Рис. 1. Зависимость V/Vмин от рН при полимеризации АК в водных растворах.
[АК] = 0,5 моль/л; [I]=2,85 10-3 моль/л; 50 °С

Рис. 2. Зависимость V/Vмин при полимеризации АК (1) и МАК (2) от рН
водного раствора, установленного добавлением NaOH. [АК] = 1,2 моль/л;
[ДАК] = 5×10-3 моль/л; Vмин = 4×10-6моль/л×с; [МАК] = 0,92 моль/л;
[ДАК] = 5×10-4 моль/л; Vмин=1,15×10-6 моль/л×с; 60 °С.
ионизованы, т.е. в реакционном растворе присутствуют только акрилат- и метакрилатанионы. ПАК и ПМАК в среднем значительно слабее соответствующих мономерных кислот и их ионизация с ростом рН происходит в щелочной области, т.е. наблюдаемым в этой области рН кинетическим эффектам сопутствует изменение химической природы растущих цепей. Возможность изменения эффективной реакционной способности макрорадикалов как раз и предусматривается данной гипотезой. Предполагается, что если ионизованные, т.е. отрицательно заряженные, макрорадикалы роста способны образовывать ионные пары с низкомолекулярными катионами, присутствующими в растворе, в частности, на концах растущих цепей, то это должно приводить к возрастанию скорости реакции роста цепи из-за снятия электростатического отталкивания между растущим радикалом и одноименно заряженным мономером. Тогда должно нивелироваться электростатическое отталкивание при сближении мономерных анионов с одноименно заряженными радикалами в актах роста цепи [19, 20].
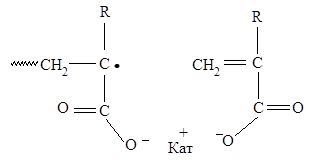
Схема 1
С ростом рН должна увеличиваться вероятность образования ионных пар на концах растущих цепей, что в рамках гипотезы должно приводить к увеличению эффективной константы скорости роста kр. Действительно, в соответствии с данными работ [15, 16], повышение концентрации ионов Na+ при данной концентрации мономера и фиксированном значении рН раствора (рН > 7) сопровождается увеличением общей скорости полимеризации [16]. (Понятие «ионная пара» используется в терминах Фуосса, т.е. предполагается непосредственный контакт сольватных оболочек противоположно заряженных ионов [20]).
Информация о химии
Uut — Ununtrium (Унунтриум)
УНУНТРИУМ (Унунтритий, ?Унунтрий?) (лат. Ununtrium), Uut, химический элемент III группы периодической системы, атомный номер 113, атомная масса [284], наиболее устойчивый изотоп 284Uut. Свойства: Радиоактивен. Металл, повидимому ...
Пневматическая химия
Недостатки теории флогистона наиболее ясно выявились в период развития т.н. пневматической химии. Крупнейшим представителем этого направления был Р.Бойль: он не только открыл газовый закон, носящий теперь его имя, но и сконструиро ...
Флори (Flory), Пол Джон
Американский химик Пол Джон Флори родился в Стерлинге, маленьком городке штата Иллинойс, в семье Эзры Флори, священника-педагога, и Марты (в девичестве Брумбау) Флори, учительницы. После получения среднего образования в местной шк ...


