Исследование твердых электролитов
Рефераты по химии / Исследование твердых электролитовСтраница 12
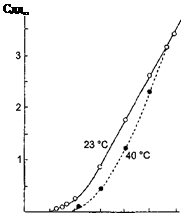
Рис 3.3.1 Кривые растворимости AgI в концентрированном растворе Кl
Разбавление достигалось несколькими способами:
а) добавлением воды, медленно поступающей сверху через стеклянную трубку в ростовую камеру, содержащую насыщенный при комнатной температуре раствор Agi в KI [9,10];
б) поступлением воды из паровой фазы, образующейся при испарении Н;0 в соседнем сосуде [11], в) принудительной подачей воды снизу в ростовую камеру через специальные мембраны [12] Указанные методики позволили получить монокристаллические образцы |3-фазы Agi размерами до 20 мм в длину и несколько миллиметров в поперечнике.
2.3.3 Раствор-расплавные методики
При кристаллизации из растворов в расплавах особое значение имеет знание фазовой диаграммы участвующих компонентов, поскольку в этом случае можно установить параметры кристаллизации, прежде всего температурный режим. Так как система расплавленных солей одновременно может содержать нейтральные молекулы, простые и комплексные ионы, то при понижении температуры в системе возможно образование эвтектик, твердых растворов или соединений.
Если в качестве растворителя используются расплавы, то растворитель и растворяемое вещество в расплавленном состоянии должны обладать полной смесимостью, но не должны образовывать твердый раствор. Наиболее пригоден растворитель, дающий с растворяемым веществом эвтектику с высоким содержанием растворителя.
Для осуществления процесса кристаллизации в расплавах солей в качестве растворителя лучше выбирать расплавы, удовлетворяющие следующим требованиям: 1) растворитель — легкодоступное химически чистое вещество; 2) растворяемое вещество имеет большой положительный температурный коэффициент растворимости; 3) растворимость вещества конгруэнтна, т.е. внутри системы не протекают химические реакции; 4) низкая упругость пара при рабочих температурах; 5) небольшая вязкость расплава; 6) невысокая агрессивность относительно материала тигля; 7) легкая растворимость растворителя в воде.
Уменьшить влияние примесей удается использованием растворителей, имеющих общие атомы с выращиваемым соединением. Для выращивания кристаллов с целью понижения рабочей температуры роста необходимо, чтобы точка плавления растворителя была как можно ниже точки плавления растворяемого вещества. В качестве растворителя применяют и смесь солей, но в этом случае образование комплексов или соединений осложняет подбор условий выращивания. При выращивании кристаллов из растворов в расплавах разумно использовать затравочные кристаллы, что ограничивает число растущих кристаллов, а рост происходит в нужной области наиболее благоприятных пересыщений.
Необходимо учитывать, что при росте кристаллов может произойти захват части растворителя (маточного раствора), особенно если осуществляется изоморфное вхождение элементов растворителя в решетку выращиваемого вещества. Для исключения этого размерные параметры компонентов должны сильно отличаться или растворитель и растворяемое вещество должны обладать общими составными частями. Экспериментальные трудности кристаллизации из растворов в расплавах определяются агрессивностью участников реакции, величиной температуры кристаллизации и точностью ее поддержания.
При кристаллизации в изотермических условиях для роста кристаллов создается локальный температурный градиент, что влечет за собой возникновение в области фисталлтоации высокого пересыщения. Алпаратурно это достигается применением охлаждаемого стержня.

Раствор-расплавный метод широко используется для получения кристаллов ТЭЛ. Рассмотрим в качестве примера рост кристаллов литийпроводящих материалов Li3М2(Р04)3 (где М = Fe, Sc) [В, 14]. В качестве растворителя использовали смесь LiF—V205, причем фторид лития здесь является и растворителем, и источником ионов Li+ для кристаллизуемого соединения. Локализация зародышеобразования происходила на вращающемся платиновом стержне, диаметром 6 мм при средней скорости охлаждения системы 0,5 град./ч. Темперарный интервал кристаллизации составлял 800-650°С Исследование фазообразования в - хтемах М205—NH4НзР04—LiF-—\/205 позволило определить температурные области устойчивости фосфатов заданных составов и найти условия монофазной кристаллизации сочинений Li2М2(Р04)з Габитус кристаллов существенно зависит от условий кристаллизации в частности, от скорости охлаждения системы) и концентрации кристаллообразующих компонентов призматические кристаллы формируются при более низких концентрациях и чалых скоростях охлаждения, а пластинчатые — при более высоких концентрациях и больших скоростях охлаждения
Информация о химии
Вычислительная химия
Вычислительная химия — ветвь химии, которая использует компьютеры для решения химических проблем. Вычислительная химия использует результаты классической и квантовой теоретической химии, реализованные в виде эффективных комп ...
Se — Селен
СЕЛЕН (лат. Selenium), Se, химический элемент VI группы периодической системы Менделеева, атомный номер 34, атомная масса 78,96. Свойства: образует несколько модификаций. Наиболее устойчив серый селен: кристаллы, плотность 4,807 ...
Мичерлих (Mitscherlich), Эйльгард
Немецкий химик Эйльгард Мичерлих родился в семье пастора небольшого селения Нёйенде на севере Германии. В 1811–1813 гг. он учился в Гейдельбергском и Парижском университетах, где изучал историю и культуру народов Востока. В ...


